從研發到上市,需時至少要一年半
無論怎麼緊急,基於醫學倫理,研發一支要打在人身上的疫苗,都有一定的過程與步驟。就算幸運之神眷顧,疫苗研發過程一路順暢,關關難過關關過,且研究機構所屬政府給予行政特許,疫苗從研發到上市,至少也要一年半的時間。
◎黃天如
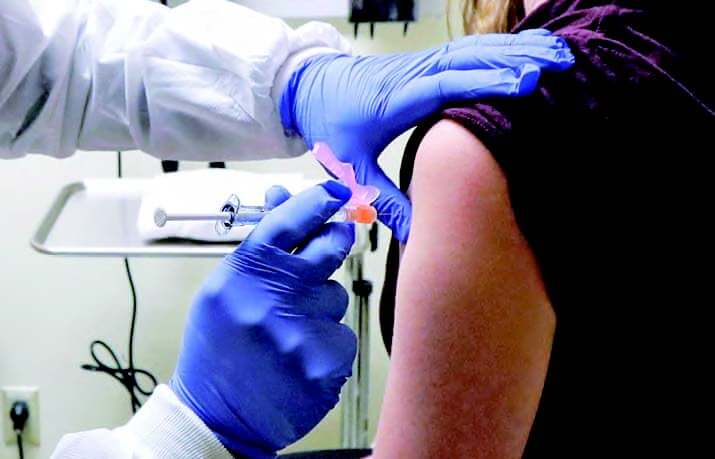
研發一支要打在人身上的疫苗,至少也要18個月的時間。
武漢肺炎(新冠肺炎)病毒衍生全球大流行,更可怕的是,武漢肺炎至今無藥可醫,更無疫苗可預防。世人對武漢肺炎疫苗引頸期待,同一時間各國研究機構也「捷報頻傳」,其中以色列某機構更言之鑿鑿地表示,他們研發的疫苗九十天後就能問世。
從研發到上市難關重重
然而,世界衛生組織(WHO)強調,研發一支要打在人身上的疫苗,即使天時地利人和皆備,外加研發國特許上市,至少也要十八個月的時間,即最快也要明年底,才有可能出現真正的好消息。
若說對抗新興病毒有三寶,恐不外乎「快篩試劑、藥物、疫苗」,只要能快速篩檢出感染者,隨即投藥治療,再配合健康者全面施打疫苗,病例數就能獲得控制,也能大幅降低重症與死亡案例的發生。
但無論再怎麼緊急,基於醫學倫理,研發一支要打在人身上的疫苗,都有一定的過程與步驟,包括:前期製備、後期試驗驗證(動物實驗及三期人體臨床試驗)、註冊、上市、量產,最終投入使用。
其中最大考驗為三期人體試驗。一般第一期多會徵求數十名健康成人參與,目的為測試疫苗最高的安全劑量;第二期會納入更多受試者,例如若疫苗未來施打族群包含兒童,此時就可能安排大齡健康兒童受試;第三期人體臨床試驗主要目的為證明疫苗的療效,一般會納入更大規模的受試者,也可能以雙盲方式(編按:試驗對象為人類時使用,目的是避免試驗的對象或進行試驗的人員主觀偏向影響實驗的結果,通常雙盲試驗得出的結果會更為嚴謹)安排安慰劑對照組。
上述過程的每一關都需要相當可觀的整備與執行時間,且一旦任何一關執行結果不理想,例如疫苗的安全性或有效性未如預期,整個計畫就得提前終止,或至少必須重頭來過。
就算幸運之神眷顧,疫苗研發過程一路順暢,關關難過關關過,且研究機構所屬政府給予行政特許,一個疫苗從研發到上市,至少也要一年半的時間。
那麼目前各國各機構針對武漢肺炎疫苗研發傳出的好消息都是在「膨風」?當然也不是。尤其多數國家的研究機構只是在報告他們預計何時完成動物實驗,或何時進入人體試驗的時間。
瑞德西韋若無授權,便無法量產
至於個別研究機構宣稱已有如光速般完成了武漢肺炎疫苗研發,或疫苗將在三個月後上市,這樣的疫苗擺在面前,恐怕也沒幾個人敢打。
疫苗最快要等明年底才有希望,那藥物呢?美國不是利用某種藥物治癒了武漢肺炎患者,而我中央研究院(中研院)、國家衛生研究院(國衛院)不也在短短兩周內,就在實驗室合成該藥了嗎?
美國在治療某位武漢肺炎重症患者時,因臨床無藥可對症下藥,情急之下嘗試了學者專家針對伊波拉(Ebola)病毒研發的臨床試驗藥物「瑞德西韋」(Remdesivir)。沒想到患者服藥後病毒量下降,最後竟然康復了。
若瑞德西韋真是武漢肺炎病毒的剋星,自是普天同慶的喜事,可惜自該名美國病患以降,至今再未傳出其他同樣因服用瑞德西韋戰勝武漢肺炎的幸運兒。
中研院院長廖俊智也證實,雖然該院有合成高純度瑞德西韋的實力,但瑞德西韋專利權屬於美國吉利德藥廠(Gilead),而該廠在台灣也申請了專利,若無授權,便無法量產;更甚者,撇開生產專利不談,一款藥在實驗室合成有很好的進展,距離實際應用仍有非常遙遠的距離。
而中研院日前宣布只花了十九天,就研發出武漢肺炎病毒的快篩試劑,那總是貨真價實的吧?
談到病毒檢驗方式或試劑,最重要的就是特異性與敏感度。其中特異性講的是該檢驗方式或試劑只能對目標病毒有反應,好比一款武漢肺炎病毒試劑若對同為冠狀病毒家族的MERS(中東呼吸症候群)病毒也有反應,就是特異性不足;敏感度則是指準確性,尤其即使檢體只有少量病毒時,仍能靈敏地顯示為陽性。
中研院快篩試劑準確率僅六成
中研究研發的武漢肺炎快篩試劑,強調只需十五至二十分鐘就能得知檢驗結果,但廖俊智日前在立法院答詢時卻坦承,該院的抗體快篩試劑準確率只有六成。
中央疫情指揮中心監測應變官莊人祥表示,目前國內各實驗室統一採用的核酸檢驗(RT-PCR)雖須耗時四小時,但除非採檢不當導致的偽陰性,若檢驗結果為陽性,則受檢者接近百分之百為感染者無誤。
閱讀完整內容



